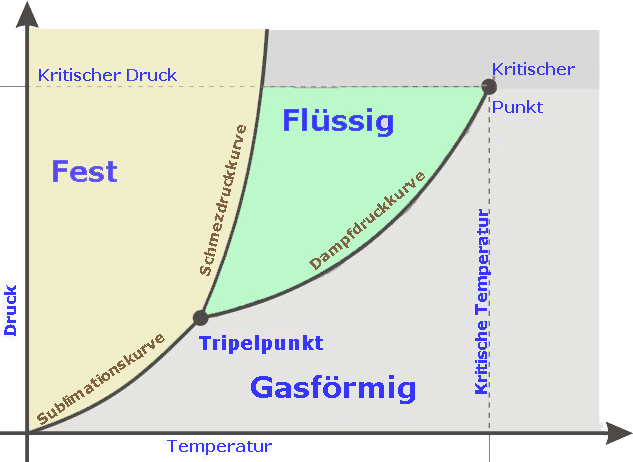
Anhand des beispielhaft aufgeführten Phasendiagramms eines reinen Stoffes, lässt sich leicht erklären, wie sich die Aggregatzustände des idealen Gases in Abhängigkeit von Druck und Temperatur verändern.
Die drei Phasen fest, flüssig, gasförmig werden durch die Phasenlinien fest/flüssig (Schmelzdruckkurve), flüssig/gasförmig (Verdampfungskurve) und fest/gasförmig (Sublimationskurve) voneinander getrennt.
Für Punkte, die exakt auf den Kurven bzw. Linien liegen (eindeutig durch Druck und Temperatur definiert) liegt der reine Stoff jeweils in zwei Phasen vor, die miteinander im Gleichgewicht stehen. Am
Tripelpunkt laufen alle drei Phasenlinien (tripel für drei) zusammen. Der Tripelpunkt ist der Punkt, wo alle drei Phasen fest, flüssig, gasförmig im Gleichgewicht koexistieren. Im
kritischen Punkt endet die Dampfdruckkurve. Zu jedem kritischen Punkt existiert somit eine
kritische Temperatur und ein
kritischer Druck (siehe hierzu auch
p V T Diagramm). Am kritischen Punkt laufen flüssige Phase und Gasphase zusammen. Da in der Nähe des kritischen Punktes die Dichteunterschiede zwischen flüssiger Phase und Gasphase sehr gering sind, wird hier auch von
fluid gesprochen. Oberhalb des kritischen Punktes besteht nur noch die Gasphase. Das Gas wird im Bereich zwischen Tripelpunkt und kritischem Punkt oft auch als
Dampf bezeichnet. Der kritische Punkt eines Gases ist exakt durch die Temperatur und den Druck definiert. Oberhalb des Kritischen Punktes kann ein Gas durch Druckerhöhung nicht mehr verflüssigt werden. Dies lässt sich im
p V T Diagramm zeigen.
Bei der technischen Gasverflüssigung wird das Gas nach dem von Karl von Linde entwickelten Verfahren bis unter die kritische Temperatur abgekühlt (Ausnutzung des
Joule-Thomson-Effektes). Solange die kritische Temperatur eines Gases nicht überschritten wird, lässt sich dieses Gas isotherm, durch Druckerhöhung oder durch isobare Abkühlung, unter dem Kondensationspunkt verflüssigen.